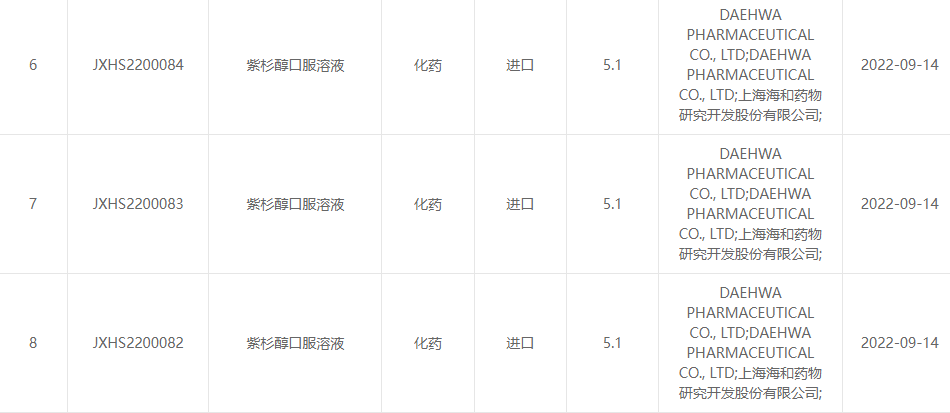
Op 13 september 2022 maakten Shanghai Haihe Pharmaceutical Research and Development Co., Ltd. en Daehwa Pharmaceutical Co., Ltd. gezamenlijk bekend dat de paclitaxel orale oplossing (RMX3001), gezamenlijk ontwikkeld door de twee partijen, officieel is goedgekeurd door het Center for Drug Evaluatie (CDE) van de State Drug Administration.(Acceptatienummer: JXHS2200082 land, JXHS2200083 land, JXHS2200084 land).
Bron afbeelding: State Drug Administration
Paclitaxelwordt veel gebruikt bij de behandeling van verschillende kwaadaardige tumoren, zoals longkanker, borstkanker, eierstokkanker, hoofd-halskanker en maagkanker.Eiwitpolymerisatie, assemblage van microtubuli, het voorkomen van depolymerisatie, waardoor microtubuli worden gestabiliseerd en de mitose van kankercellen wordt geremd en apoptose wordt teweeggebracht, waardoor de proliferatie van kankercellen effectief wordt voorkomen en een antikankereffect wordt gespeeld.
Momenteel gebruiken de meeste delen van de wereld paclitaxel in de vorm van een injectie, die moet worden geformuleerd en toegediend via een intraveneus infuus in het ziekenhuis.Patiënten moeten regelmatig naar het ziekenhuis terugkeren en er zullen bijwerkingen optreden op de injectieplaats.Daarom is de ontwikkeling van orale paclitaxelpreparaten altijd een hotspot geweest in industrieel onderzoek..
RMX3001 is een orale formulering van paclitaxel ontwikkeld door Dahua Pharmaceutical op basis van zijn innovatieve, zelf-emulgerende medicijnafgiftetechnologie.Het is in september 2016 goedgekeurd door de Koreaanse Food and Drug Administration (handelsnaam Liporaxel) en de indicatie is geavanceerde of tweedelijnsbehandeling van gemetastaseerde maagkanker of lokaal recidiverende maagkanker.Volgens een persbericht van Haihe Pharmaceuticals is Liporaxel het eerste orale paclitaxelproduct dat tot nu toe met succes is ontwikkeld en goedgekeurd voor marketing in de wereld.In september 2017 verwierf Haihe Pharmaceutical de R&D-, productie- en verkooprechten van het product op het vasteland van China, Hong Kong, Taiwan en Thailand van Dahua Pharmaceuticals.
De registratieaanvraag voor RMX3001 in China is voornamelijk gebaseerd op een gerandomiseerde, open-label, parallel gecontroleerde, non-inferioriteitsopzet, multicenter fase 3 klinische studie, die tot doel heeft de tweedelijnsbehandeling van paclitaxel drank RMX3001 te vergelijken met Paclitaxel-injectie (Taxol) Werkzaamheid en veiligheid bij patiënten met gevorderde maagkanker.De studie werd gezamenlijk uitgevoerd door professor Li Jin van het Shanghai Oriental Hospital en professor Qin Shukui van het Nanjing Jinling Hospital als hoofdonderzoekers.
Dr. Ruiping Dong, Chief Executive Officer van Haihe Pharmaceuticals, zei: “De aanvaarding van de aanvraag voor paclitaxel drank (RMX3001) is een nieuwe belangrijke mijlpaal voor Haihe Pharmaceuticals, en ik ben de klinische onderzoekers en patiënten die hebben deelgenomen aan onze proces.Geavanceerde maagkanker Er is nog steeds een enorme onvervulde klinische behoefte aan behandeling, en we hopen de meest geavanceerde, innovatieve en handige behandelingen ter wereld zo snel mogelijk aan patiënten in China en de rest van de wereld te kunnen aanbieden.”
Yunnan Hande Biotechnology Co., Ltd. richt zich al 28 jaar op de productie van paclitaxel.Het is 's werelds eerste onafhankelijke fabrikant van het plantaardige kankermedicijn paclitaxel dat is goedgekeurd door de Amerikaanse FDA, de Europese EDQM, de Australische TGA, de Chinese CFDA, India, Japan en andere nationale regelgevende instanties.onderneming.Als je wilt kopenPaclitaxel-API,Neem dan online contact met ons op.
Posttijd: 14 september 2022